Chemická reakcia predstavuje proces, pri ktorom dochádza k zmenám v zložení a štruktúre látok. Látky, ktoré vstupujú do reakcie, nazývame reaktanty, zatiaľ čo látky, ktoré reakciou vznikajú, sa označujú ako produkty.
Zmenu reaktantov na produkty je možné vyjadriť pomocou chemickej rovnice, ktorá slúži ako stručný symbolický zápis chemickej reakcie. Počas každej reakcie dochádza k rozrušeniu starých väzieb a vytvoreniu nových.
Delenie chemických reakcií
Chemické reakcie môžeme klasifikovať podľa rôznych kritérií:
Podľa celkovej zmeny:
- Syntetické reakcie: Pri týchto reakciách z niekoľkých reaktantov vzniká jeden produkt. Napríklad: S + O2 → SO2.
- Rozkladné reakcie: V tomto prípade z jedného reaktantu vzniká niekoľko produktov. Napríklad: CaCO3 → CaO + CO2.
- Substitučné reakcie: Pri týchto reakciách jeden prvok v zlúčenine nahrádza iný. Napríklad: CuSO4 + Fe → FeSO4 + Cu.
Podľa mechanizmu reakcií (v anorganickej chémii):
- Protolytické reakcie: Tieto reakcie prebiehajú medzi kyselinami a zásadami a sú založené na výmene protónov.
- Redoxné reakcie: Pri týchto reakciách dochádza k výmene elektrónov a zmene oxidačných čísel atómov.
- Zrážacie reakcie: Pri nich vzniká málo rozpustná alebo nerozpustná zrazenina.
- Komplexotvorné reakcie: Pri nich vznikajú komplexné (koordinačné) zlúčeniny.
Podľa energetickej bilancie:
- Exotermické reakcie: Pri týchto reakciách sa uvoľňuje energia (ΔH < 0). Napríklad: N2 + 3H2 → 2NH3 (ΔH = - 92,4 kJ).
- Endotermické reakcie: Tieto reakcie spotrebúvajú energiu (ΔH > 0). Napríklad: CaCO3 → CaO + CO2 (ΔH = + 178 kJ).
Podľa javového opisu organických látok:
- Adičné reakcie: Dochádza k zlučovaniu dvoch alebo viacerých častíc na jednu zložitejšiu, pričom zaniká násobná väzba. Napríklad: CH2=CH2 + Br2 → CH2Br-CH2Br.
- Eliminačné reakcie: Jedna častica sa štiepi na viac jednoduchších, pričom vzniká násobná väzba. Napríklad: CH3-CH3 - H2 → CH2=CH2.
- Substitučné reakcie: Dochádza k zániku jednej a vzniku druhej väzby na tom istom atóme. Napríklad: CH4 + Cl2 → CH3Cl + HCl.
- Prešmyky: Ide o premiestnenie atómov, skupín alebo častí uhlíkového reťazca.
Podľa fázy v reakčnej sústave:
- Homogénne reakcie: Reaktanty aj produkty sú v rovnakej fáze, napríklad v roztoku.
- Heterogénne reakcie: Reaktanty a produkty sú v rôznych fázach.

Protolytické reakcie
Protolytické reakcie sú reakcie medzi kyselinami a zásadami, kde dochádza k výmene protónov (H+). Kyselina je látka schopná odovzdávať protón (donor), zatiaľ čo zásada je schopná protón prijať (akceptor).
Disociácia kyselín a zásad vo vode:
- Disociácia kyselín: Kyselina reaguje s vodou za vzniku oxóniových katiónov (H3O+) a aniónu kyseliny. Napríklad: HA + H2O ⇌ A⁻ + H3O⁺. Sila kyseliny sa vyjadruje disociačnou konštantou (KA).
- Disociácia zásad: Zásada reaguje s vodou za vzniku amónnych katiónov (HB⁺) a hydroxidových aniónov (OH⁻). Napríklad: B + H2O ⇌ HB⁺ + OH⁻. Sila zásady sa vyjadruje disociačnou konštantou (KB).
Autoprotolýza vody:
Voda má amfotérny charakter, čo znamená, že môže reagovať ako kyselina aj ako zásada. Vzájomnou reakciou dvoch molekúl vody vznikajú oxóniové a hydroxidové ióny: H2O + H2O ⇌ H3O⁺ + OH⁻. Tento proces sa nazýva autoprotolýza vody a vedie k ustaveniu rovnováhy, ktorá je charakterizovaná iónovým súčinom vody (Kv). V čistej vode platí, že koncentrácia H3O⁺ a OH⁻ iónov je rovnaká, čo znamená, že roztok je neutrálny. V kyslých roztokoch je koncentrácia H3O⁺ vyššia ako OH⁻, zatiaľ čo v zásaditých roztokoch je to naopak.
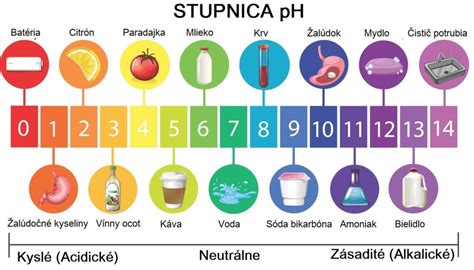
Pre lepšie vyjadrenie kyslosti a zásaditosti sa používa pH stupnica: pH = - log [H3O⁺].
Neutralizácia:
Neutralizácia je reakcia vodného roztoku kyseliny a zásady, pri ktorej vzniká soľ a voda. Napríklad: HCl + NaOH → NaCl + H2O. Tento proces má význam napríklad pri likvidácii kyslých a zásaditých odpadových vôd.
Hydrolýza solí:
Hydrolýza solí je protolytická reakcia iónov soli s vodou. V závislosti od sily kyseliny a zásady, od ktorej soľ pochádza, môže byť výsledný roztok neutrálny, kyslý alebo zásaditý.
Zrážacie reakcie
Pri zrážacích reakciách sa aspoň jeden z produktov vylúči vo forme málo rozpustnej alebo úplne nerozpustnej zrazeniny. Malá rozpustnosť je daná silnými príťažlivými silami medzi iónmi. Tieto reakcie sa využívajú napríklad v analytickej chémii na dôkazové reakcie.
Príklad: AgNO3 + NaCl → AgCl↓ + NaNO3.

Redoxné (oxidačno-redukčné) reakcie
Redoxné reakcie sú charakterizované výmenou elektrónov medzi reaktantmi, čo sa prejavuje zmenou oxidačných čísel atómov. Delia sa na dve čiastkové reakcie:
- Oxidácia: Reagujúca častica odovzdáva elektróny a zvyšuje svoje oxidačné číslo.
- Redukcia: Reagujúca častica prijíma elektróny a znižuje svoje oxidačné číslo.
Oxidácia a redukcia prebiehajú vždy súčasne.
Oxidačné a redukčné činidlá:
- Oxidačné činidlá (oxidanty): Látky schopné oxidovať iné látky, pričom sa samy redukujú (napr. O2, Cl2, MnO4⁻).
- Redukčné činidlá (reduktanty): Látky schopné redukovať iné látky, pričom sa samy oxidujú (napr. prvky s nízkou elektronegativitou, ióny kovov s nízkym oxidačným číslom).
Oxidačné číslo je formálny elektrický náboj prvku v zlúčenine.

Elektrolýza
Elektrolýza je proces, pri ktorom sa elektrický prúd využíva na vyvolanie chemickej reakcie v elektrolyte. Na elektródach (katóde - redukcia, anóde - oxidácia) prebiehajú redoxné procesy.
Komplexotvorné reakcie
Tieto reakcie vedú k vzniku komplexných (koordinačných) zlúčenín. Komplexná zlúčenina sa skladá z centrálneho atómu, na ktorý sú prostredníctvom donor-akceptorovej väzby viazané ligandy. Koordinačné číslo udáva počet atómov alebo skupín viazaných na centrálny atóm.
Príklad komplexného katiónu: [Cu(H2O)4]²⁺, kde Cu je centrálny atóm a H2O sú ligandy.
Typy chemických reakcií
Chemické reakcie sú základným kameňom chémie, umožňujúcim pochopenie premeny látok a ich využitie v praxi.